Ученые создали первое биоинженерное сердце человека с функционирующей сердечной мышцей
 1966
1966 0
0
Исследователи из Главного Госпиталя Массачусетса (Massachusetts General Hospital, MGH, США) сделали первые важные шаги в направлении создания биоинженерного человеческого сердца с использованием донорского сердца, лишенного компонентов, которые способны вызвать иммунный ответ, а также клеток сердечной мышцы, полученных из индуцированных плюрипотентных стволовых клеток (ИПСК), которые потенциально можно получить от будущих реципиентов. Результаты и методы исследования, включая разработку автоматизированной системы биореактора, способного поддерживать тканевой каркас человеческого сердца в тот момент, когда из него удаляют клетки, были опубликованы в журнале Circulation Research.
«Создание функциональной сердечной ткани включает в себя решение целого ряда проблем, в частности, получение структурной подложки, способной поддерживать сердечную функцию, поступление специализированных клеток сердца и благоприятную окружающую среду, в которой клетки могут заселить подложку и сформировать впоследствии зрелую ткань, способную выполнять сложные функции сердца», – говорит Жак Гуйтте (Jacques Guyette) из Центра регенеративной медицины при MGH (MGH Center for Regenerative Medicine, CRM), один из авторов исследования.
Исследовательской группой руководил доктор Харальд Отт (Harald Ott) из MGH CRM и кафедры хирургии. В 2008 г. Отт разработал метод, позволяющий удалять живые клетки из донорского органа с помощью раствора детергента, а затем заново заселять оставшийся внеклеточный матрикс подложки соответствующим типом клеток. С тех пор его команда использовала этот метод для создания функциональных почек и легких у крыс, а также для удаления клеток из сердца, легких и почек крупных животных. В новой статье впервые приводится детальное описание подложки, оставшейся после удаления клеток из целого человеческого сердца. Кроме того, ученые описывают процесс повторного заселения матрикса трехмерных и целых сердец сердечными клетками.
В исследование было включено 73 человеческих сердца, предоставленных банком органов New England Organ Bank в связи с непригодностью для трансплантации. Имелись донорские сердца людей с погибшим головным мозгом и донорские сердца людей, умерших из-за сердечно-сосудистых заболеваний. Сперва исследовательская команда удалила все клетки из сердец; детальная характеристика оставшихся сердечных каркасов подтвердила высокое удерживание матриксных белков и структур, свободных от клеток сердца, сохранение коронарных сосудов и микрососудистых структур, а также освобождение каркасов от лейкоцитарных антигенов человека, которые могут вызвать реакцию отторжения трансплантата. Результаты исследования показали, что органы из двух донорских групп практически одинаково отреагировали на сложный процесс удаления из них клеток.
Вместо применения генетических манипуляций для получения ИПСК из клеток взрослого организма, исследовательская команда использовала новый метод, позволяющий репрограммировать клетки кожи с помощью факторов матричной РНК, что является более эффективным методом репрограммирования и вызывает меньше трудностей при регуляции процесса. Затем ученые дифференцировали плюрипотентные клетки в клетки сердечной мышцы (кардиомиоциты), зафиксировав паттерны экспрессии генов, отражающие этапы развития, и создав клеток в необходимом количестве, достаточном для их клинического применения. После этого кардиомиоциты были пересажены в трехмерную матричную ткань: сначала на тонкие слои матрикса, а затем на 15 мм волокна, которые через несколько дней культивирования превратились в спонтанно сокращающиеся ткани.
Последний этап исследования демонстрирует первый случай регенерации человеческой сердечной мышцы из плюрипотентных стволовых клеток в бесклеточном матриксе целого человеческого сердца. Исследовательская команда трансплантировала около 500 миллионов кардиомиоцитов, полученных из ИПСК, в стенку левого желудочка сердца, предварительно лишенного клеток. В течение 14 дней органы находились в автоматизированной системе биореактора, разработанной научной группой из MGH. Это позволило одновременно проводить перфузию органа питательным раствором и воздействовать на него стрессовыми экологическими факторами, например, воспроизводить такие же условия работы, как и у живого сердца, в частности, давление желудочков. Анализ регенерировавшей ткани показал наличие плотных участков клеток, полученных из ИПСК, которые имели вид незрелой сердечной мышечной ткани и функционально сокращались в ответ на электрическую стимуляцию.
«Восстановление целого сердца, безусловно, является долгосрочной целью, к которой мы начнем приближаться через несколько лет, поэтому в настоящее время мы работаем над созданием функционального фрагмента миокарда, который мог бы заменить поврежденную сердечную ткань при инфаркте или сердечной недостаточности. В будущем мы планируем усовершенствовать методы, которые позволят нам получить еще больше сердечных клеток, поскольку повторное заселение клетками целого сердца потребует десятков миллиардов клеток, а также оптимизировать методы культивирования в биореакторе для улучшения созревания и функции созданной сердечной ткани, а также разработать электронную интеграцию регенерировавшей функционирующей ткани в сердце реципиента», – говорит Гуйтте.
«Создание персонализированного функционального миокарда из клеток пациента является важным шагом на пути к новым аппаратно-инженерным стратегиям, этот метод позволит смоделировать заболевания конкретного пациента и разработать новую терапию. Наша исследовательская команда готова разрабатывать эти стратегии в своих будущих проектах», – говорит научный руководитель исследовательской команды Харальд Отт, доцент кафедры хирургии из Гарвардской Медицинской Школы (Harvard Medical School, США).
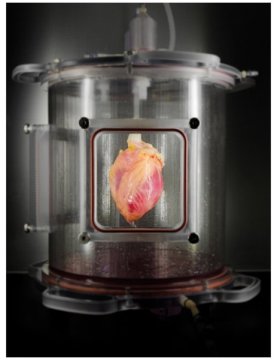
Сердце человека, частично заново заселенное человеческими кардиомиоцитами, полученными из индуцированных плюрипотентных стволовых клеток. Сердце культивируется в биореакторе, который обеспечивает поступление питательного раствора и воспроизводит некоторые из условий окружающей среды сердца. (фото: Bernhard Jank, MD, Ott Lab, Center for Regenerative Medicine, Massachusetts General Hospital)
По материалам Massachusetts General Hospital
Оригинальная статья:
Jacques P. Guyette, Jonathan M. Charest, Robert W. Mills, Bernhard J. Jank, Philipp T. Moser, Sarah E. Gilpin, Joshua R. Gershlak, Tatsuya Okamoto, Gabriel Gonzalez, David J. Milan, Glenn R. Gaudette, Harald C. Ott. Bioengineering Human Myocardium on Native Extracellular MatrixNovelty and Significance. Circulation Research, 2016; 118 (1): 56 DOI: 10.1161/CIRCRESAHA.115.306874





