Из стволовых клеток созданы рудиментарные яйцеклетки и сперматозоиды
 2280
2280 0
0
Исследователи из Израиля и Великобритании получили в лаборатории предшественники сперматозоидов и яйцеклеток человека, используя клетки кожи, репрограммированные в стволовое состояние. Это достижение – небольшой шаг вперед в лечении бесплодия, несмотря на то, что результаты могут вызвать значительные противоречия и законодательные сложности.
В ходе эксперимента, результаты которого сообщаются в интернет-публикации журнала Cell [1], исследователям удалось воспроизвести на клетках человека процедуру, ранее разработанную на мышиных клетках, в ходе которой индуцированные плюрипотентные стволовые клетки (ИПСК) – репрограммированные в стволовое состояние клетки, способные дифференцироваться почти в любой клеточный тип – использовались для получения сперматозоидов или яйцеклеток, которые впоследствии могут подвергнуться процедуре искусственного оплодотворения для рождения ребенка.
В 2012 г. специалист в области стволовых клеток Митинори Саиту (Mitinori Saitou) из Университета Киото (Kyoto University, Япония) и его коллеги создали первые искусственные примордиальные половые клетки (ППК, предшественники половых клеток человека) [2]. Это специализированные клетки, возникающие на этапе эмбрионального развития и дающие начало сперматозоидам или яйцеклеткам. Саиту создал их «в пробирке», используя клетки кожи, репрограммированные в эмбрионально-подобное состояние через технологию ИПСК. Исследователям удалось добиться таких же результатов, используя эмбриональные стволовые клетки (ЭСК).
Несмотря на то, что полученные клетки не были способны к делению дальше стадии предшественников, Саиту обнаружил, что помещение клеток-предшественниц в семенники мыши может способствовать их развитию в сперматозоиды, а помещение в яичники – формированию функциональных яйцеклеток. Оба полученных типа половых клеток можно использовать для экстракорпорального оплодотворения (ЭКО).
Попытки получения аналогичных функциональных гамет у человека привели к созданию клеток, подобных ППК, но с довольно низкой эффективностью (уровнем превращения стволовых клеток в половые), что оказалось препятствием для дальнейшего расширения работы. Кроме того, предыдущий подход требовал внедрения генов, что делало невозможным использование клеток в клинике.
Теперь группа под руководством Азим Сурани (Azim Surani) из Университета Кембриджа (University of Cambridge, Великобритания) и Джакоба Ханна (Jacob Hanna) из Института Наук Вейцмана (Weizmann Institute of Science, Израиль) воспроизвела «первую половину» (in vitro-часть) эксперимента Саиту на клетках человека.
Высокая эффективность
Ключевым в успехе биологов стало обнаружение правильной отправной точки. Основной проблемой для повтора успеха с клетками человека являлось существенное различие между ЭСК человека и мыши. ЭСК грызуна «наивные» – их легко перенаправить на любой путь дифференцировки, в то время как стволовые клетки человека «подготовлены», что делает их менее адаптируемыми.
Однако Ханна понял, что эти различия можно преодолеть, «откорректировав» клетки, о чем он с коллегами сообщил в публикации 2013 г. [3]. Исследователи разработали способ превращения ЭСК человека в «наивные», как у мышей.
«При первом же использовании этих клеток с протоколом Саиту мы получили ППК с высокой эффективностью», – рассказывает ученый.
Работая совместно, Сурани и Ханна использовали ЭСК и ИПСК мужчин и женщин для получения клеток-предшественниц гамет с эффективностью 25-40%.
«Очень интересно, что лаборатории Сурани и Ханна нашли способ создания прогениторных половых клеток с самой большой эффективностью», – отмечает Амандер Кларк (Amander Clark), эксперт по биологии репродукции в Калифорнийском Университете (University of California, США).
Полученные клетки несут множество меток ППК. В частности, их эпигенетический паттерн – химические модификации хромосом, влияющие на экспрессию генов – схож с таковым у ППК. Исследовательская группа сравнила белковые маркеры искусственных примордиальных половых клеток с естественными, полученными из абортивных плодов, и обнаружила их значительное сходство.
По словам Саиту, будут предприниматься дальнейшие попытки понять и контролировать процесс получения клеток. В частности, похоже, что в клетках человека ключевую роль играет белок SOX17, тогда как у мышей она же выполняется белком Sox2.
Следующим шагом работы на мышах стало внедрение искусственных ППК в семенники или яичники животных для развития их в функциональные половые клетки.
Однако, по словам Ханна, он и его коллеги еще не готовы для подобных действий на человеке. Другие исследователи также соглашаются, что еще многое остается неизвестным для введения искусственных ППК в организм человека.
По мнению Ханна, ученые также рассматривают возможность инъецирования искусственных ППК человека в семенники или яичники мышей и других животных, или же они попытаются провести весь эксперимент на приматах. Ученый считает, что продолжение экспериментов Саиту и других коллег по завершению процесса развития мышиных сперматозоидов и яйцеклеток в культуре может привести к формированию подхода, который можно будет подкорректировать для человека.
«Я все еще в раздумьях. После публикации статьи мы посмотрим на реакцию научного сообщества», – говорит Ханна.
По мнению Кларк, необходимо законодательство, касающееся экспериментов с клетками человека для продвижения технологии в клинику и потенциальной возможности восстановления фертильности некоторых стерильных мужчин и женщин. Например, в США законодательство запрещает федеральное финансирование проектов по созданию эмбрионов человека в исследовательских целях – то, что может быть необходимо для проверки новой технологии. Ограничения необходимо сдвинуть и заменить универсальным руководством по безопасности и этичности исследований, считает Кларк.
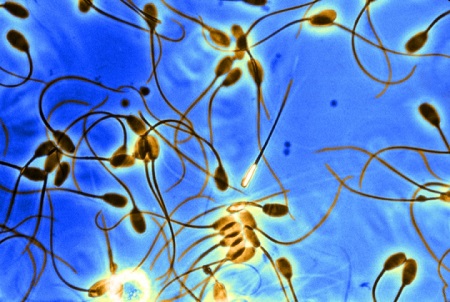
Существует надежда, что однажды из клеток кожи стерильного мужчины можно будет получить сперматозоиды, а сходный процесс позволит получить яйцеклетки из организма стерильной женщины. (Southern Illinois University/Science photo Library)
По материалам NatureNews
Оригинальная статья: Nature doi:10.1038/nature.2014.16636
Литература:
1. Irie, N. et al. Cell http://dx.doi.org/10.1016/j.cell.2014.12.013 (2015).
2. Kee, K., Angeles, V. T., Flores, M., Nguyen, H. N. & Reijo Pera, R. A. Nature 462, 222–225 (2009).
3. Gafni, O. et al. Nature 504, 282–286 (2013).





