Ученые создали генетически модифицированных комаров, блокирующих перенос малярии
 1730
1730 0
0
Ученые из Калифорнийского Университета в Ирвайне (University of California, США), используя инновационный метод генного редактирования, создали штамм комаров, способных быстро внедрить в популяцию этих насекомых через их потомство ген, препятствующий передаче малярии, что подавляет способность комаров передавать инфекционное заболевание человеку. Результаты исследования были опубликованы в журнале Proceedings of the National Academy of Sciences.
Малярия – одна из главных проблем здравоохранения в мире. Более 40% населения мира проживает в районах, где существует риск заражения заболеванием. По данным Центров по Контролю и Профилактике Заболеваний (Centers for Disease Control & Prevention, CDC, США), ежегодно регистрируется от 300 до 500 млн. новых случаев заражения малярией. Каждый год от этого заболевания умирает около 1 млн. человек, главным образом, младенцы, маленькие дети и беременные женщины, большинство из которых живет в Африке.
Разработанная американскими учеными стратегия – значимое достижение в области создания противомалярийной популяции комаров, способной в будущем искоренить заболевание.
Чтобы создать противомалярийную популяцию комаров, исследователи из кампусов Калифорнийского Университета в Ирвайне и Cан-Диего внедрили фрагмент ДНК в клетки зародышевой линии комаров Anopheles stephensi, что привело к передаче гена, предотвращающего малярию, 99,5% их потомства. А. stephensi является главным переносчиком малярии в Азии.
Исследование подчеркивает растущую значимость метода CRISPR-Cas9, мощного инструмента генного редактирования, позволяющего получить доступ к ядру клетки и разрезать ДНК, чтобы затем заменить мутантные гены или внедрить новые гены.
По мнению Энтони Джеймса (Anthony James), почетного профессора молекулярной биологии и биохимии, а также микробиологии и молекулярной генетики из UCI, полученные данные свидетельствуют о возможности применения этого метода для уничтожения малярии.
В течение почти 20 лет лаборатория Джеймса пыталась создать комаров, препятствующих распространению заболевания. Его модели лихорадки денге были протестированы во время клинических испытаний в Мексике, а в 2012 г. он помог показать, что антитела, которые нарушают биологию паразита, полученные из иммунной системы мышей, можно внедрить в комаров. К сожалению, эта характеристика передавалась по наследству только половине потомства комаров.
Ранее в этом году биологи Итан Бьер (Ethan Bier) и Валентино Ганц (Valentino Gantz) из Калифорнийского Университета в Сан-Диего (UC San Diego, США), работающие на плодовых мушках, объявили о разработке нового метода, позволяющего внедрить нужные мутации в обе копии гена. Метод подразумевал использование CRISPR-ассоциированного фермента Cas9 нуклеазы и позволил передать мутации через зародышевую линию с частотой наследования 95%.
Две исследовательские команды работали вместе над тем, чтобы соединить метод Бьера и Ганца с комарами, полученными Джеймсом. Ганц создал CRISPR-кассету с антималярийными генами, ферментом Cas9 (который разрезает ДНК в специфичном месте) и РНК-«гидом» (который направляет специфическое расщепление ДНК), которая при введении в эмбрион комара таргетно воздействует на высоко специфичную область зародышевой линии ДНК и внедряет в нее гены противомалярийных антител.
Чтобы убедиться в том, что элемент, несущий противомалярийные антитела, достиг нужной области ДНК, ученые включили в кассету белок, который передал потомству способность к красной флуоресценции в глазах. Почти 100% потомства, а точнее – 99,5%, унаследовали эту характеристику. По мнению Джеймса, это очень хороший результат для метода, способного изменить наследуемые характеристики организма.
По словам ученого, необходимо провести дальнейшие исследования, чтобы подтвердить эффективность антител, а это может, в конечном итоге, помочь начать полевые исследования. «Это – важный первый шаг. Мы знаем, что ген работает. Созданные нами комары не являются окончательной разновидностью, но мы знаем, что эта технология позволяет эффективно создавать большие популяции насекомых», – говорит Джеймс, член Национальной Академии Наук (National Academy of Sciences, США).
По словам Бьера, профессора биологии в Калифорнийском Университете в Сан-Диего, способность CRISPR-Cas9 системы нести генетический груз большого размера должна в будущем иметь масштабные области применения.
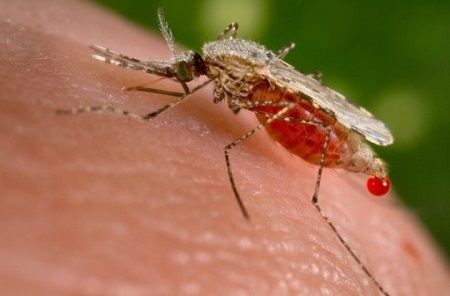
Комар Anopheles stephensi питается кровью человека. Хорошо известная ось распространения малярии, в черте которой могут быть найдены комары этого вида, простирается от Египта до Китая. (фото: Jim Gathany / CDC)
По материалам University of California, Irvine
Оригинальная статья:
Valentino M. Gantz, Nijole Jasinskiene, Olga Tatarenkova, Aniko Fazekas, Vanessa M. Macias, Ethan Bier, Anthony A. James. Highly efficient Cas9-mediated gene drive for population modification of the malaria vector mosquitoAnopheles stephensi. Proceedings of the National Academy of Sciences, 2015; 201521077 DOI: 10.1073/pnas.1521077112





