Лимфоциты-мутанты, антитела и иммунитет
 3713
3713 0
0
Лимфоциты млекопитающих производят огромное количество разнообразных антител – защитных белков, избирательно связывающихся со всевозможными чужеродными молекулами (антигенами). Способность вырабатывать иммунитет к новым инфекциям основана на внесении в гены антител случайных изменений – мутаций и последующем размножении тех лимфоцитов, у которых мутации оказались наиболее удачными. В опытах с трансгенными мышами американские ученые показали, что мутирование генов антител начинается с целенаправленной замены цитозинов урацилами, после чего в результате неточной репарации (починки) ДНК мутации распространяются в обе стороны от каждого урацила на расстояние до 30 нуклеотидов.
B-лимфоциты человека и других млекопитающих способны синтезировать миллионы разнообразных антител. Как и все прочие белки, антитела синтезируются на основе «инструкций», записанных в генах. Однако число генов в геноме млекопитающих на много порядков меньше, чем число типов антител, производимых организмом в течение жизни. Организм не может запастись заранее всеми необходимыми генами антител по двум причинам: во-первых, такое количество генов не поместится ни в каком геноме (это привело бы к непомерному росту «расходов» на содержание в каждой клетке громадного количества ДНК), во-вторых, как бы ни был велик запас защитных генов, в любой момент может появиться новая инфекция, для борьбы с которой не подойдет ни одно из имеющихся антител.
Позвоночные животные решили эту проблему, выработав специальные механизмы для прижизненного редактирования своего генома. В частности, гены антител формируются в геноме B-лимфоцитов по мере необходимости из специальных «заготовок» (гены антител в норме не передаются по наследству – наследуются только «заготовки»). Этот творческий процесс основан на тех же принципах, что и биологическая эволюция, – на случайных мутациях и избирательном размножении удачных вариантов. Впрочем, в обоих случаях «случайность» мутаций – понятие весьма относительное. Оно означает лишь, что клетка не может знать заранее, к какому результату приведет та или иная конкретная мутация. Однако клетка вполне способна контролировать скорость мутагенеза и его приуроченность к тем или иным участкам генома. Редактирование генома, таким образом, осуществляется по принципу «оптимизированного случайного поиска».
Формирование генов антител в геноме B-лимфоцитов происходит в два этапа. Сначала, на ранних стадиях развития организма, гены антител формируются комбинаторным путем из унаследованного от родителей набора заготовок (подробнее см. здесь). Каждый B-лимфоцит продуцирует только один тип антител. На этом этапе неизбежно возникают «неудачные» лимфоциты, опасные для организма: они производят аутоантитела, атакующие собственные антигены (молекулы) организма. Такие лимфоциты выбраковываются, остальные сохраняются и размножаются. В результате животное получает большой набор B-лимфоцитов (и, соответственно, антител), способных атаковать почти любые молекулы, кроме тех, которые в норме присутствуют в данном организме.
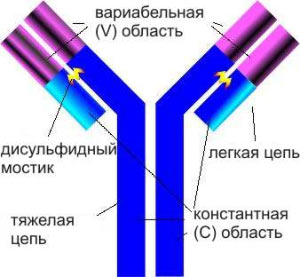 Антитело состоит из четырех белковых молекул – двух больших, или «тяжелых» цепей и двух маленьких («легких»). Вариабельная область отвечает за связывание антигена. Когда в организм попадает инфекция, гены антител подвергаются более тонкой «настройке». Те лимфоциты из имеющегося набора, чьи антитела проявляют наибольшее сродство к новому чужеродному антигену, начинают вносить случайные изменения в гены своих антител (точнее, в определенные участки этих генов – так называемые вариабельные области, или V-области). Этот процесс называется соматическим гипермутированием. Получающиеся новые варианты генов экспрессируются (то есть на их основе синтезируются антитела) и проверяются на эффективность, то есть на степень сродства к новому антигену. Это продолжается до тех пор, пока не будет найден высокоэффективный вариант гена, обеспечивающий надежную защиту от нового возбудителя. Лимфоциты, производящие такое антитело, начинают усиленно размножаться. После выздоровления некоторые из них могут долго сохраняться в качестве клеток «иммунной памяти», что снижает риск повторного заболевания.
Антитело состоит из четырех белковых молекул – двух больших, или «тяжелых» цепей и двух маленьких («легких»). Вариабельная область отвечает за связывание антигена. Когда в организм попадает инфекция, гены антител подвергаются более тонкой «настройке». Те лимфоциты из имеющегося набора, чьи антитела проявляют наибольшее сродство к новому чужеродному антигену, начинают вносить случайные изменения в гены своих антител (точнее, в определенные участки этих генов – так называемые вариабельные области, или V-области). Этот процесс называется соматическим гипермутированием. Получающиеся новые варианты генов экспрессируются (то есть на их основе синтезируются антитела) и проверяются на эффективность, то есть на степень сродства к новому антигену. Это продолжается до тех пор, пока не будет найден высокоэффективный вариант гена, обеспечивающий надежную защиту от нового возбудителя. Лимфоциты, производящие такое антитело, начинают усиленно размножаться. После выздоровления некоторые из них могут долго сохраняться в качестве клеток «иммунной памяти», что снижает риск повторного заболевания.Соматическое гипермутирование – процесс во многом загадочный. До сих пор о его механизмах было известно немногое. Было установлено, что в нём участвует особый фермент – цитидин-дезаминаза, индуцируемая активацией (activation induced (cytidine) deaminase, AID). Этот фермент атакует нуклеотиды Ц (цитозины) в V-области и отрывает от них аминогруппу (–NH2), превращая их тем самым в урацилы (У). После этого в окрестностях урацилов начинают появляться мутации (замены нуклеотидов). Мутагенез осуществляется при помощи систем репарации (починки) и репликации (удвоения, размножения) ДНК, которые в данном случае работают с большим количеством «ошибок». Многое оставалось неясным: в частности, было неизвестно, насколько необходимым является дезаминирование цитозинов для инициации гипермутирования; зависит ли число и характер мутаций от того, какой именно из цитозинов будет дезаминирован; распространяются ли мутации в обе стороны от дезаминированного цитозина или только в одну и т. д.
Чтобы прояснить детали этого процесса, биологи из Йельского университета (США) создали трансгенных мышей, которым в V-области генов антител были вставлены искусственно синтезированные фрагменты ДНК длиной в 100 нуклеотидов. Всего было использовано 4 таких фрагмента, каждый из которых вставлялся в геном одной из линий трансгенных мышей. В двух случаях из четырех фрагмент состоял только из нуклеотидов А и Т. В двух других в нём имелся один нуклеотид Ц и, соответственно, комплементарный ему нуклеотид Г в противоположной (комплементарной) цепи двухцепочечной молекулы ДНК. Фрагменты были вставлены таким образом, что у одних мышей ключевой нуклеотид Ц оказался в «нижней» (кодирующей) цепи ДНК, на основании которой синтезируется белок, а у других – в «верхней» (некодирующей).
Из B-лимфоцитов взрослых мышей выделяли ДНК и смотрели, какие мутации и в каком количестве появились во внедренном фрагменте. Оказалось, что если фрагмент не содержал нуклеотида Ц, то мутации в нём возникали лишь по краям – там, где расстояние до ближайшего Ц (расположенного за пределами внедренного фрагмента) не превышало 30 нуклеотидов. В центральной части вставленного участка ДНК мутации отсутствовали вовсе. Это означает, что присутствие цитозинов абсолютно необходимо для запуска процесса гипермутирования, и мутации распространяются лишь на небольшое расстояние от каждого Ц.
Если в середине фрагмента был нуклеотид Ц, расположенный в «верхней», некодирующей цепи ДНК, то мутации возникали в большом количестве по всей длине фрагмента. Однако если нуклеотид Ц оказывался в «нижней», кодирующей цепи, а в «верхней» напротив него располагался комплементарный ему нуклеотид Г, мутации не происходили (или заменялась только сама пара ГЦ, а окружающие ее нуклеотиды А и Т все оставались на своих местах). Таким образом, выяснилось, что сигналом для запуска процесса гипермутирования может служить только нуклеотид Ц, расположенный в «верхней» цепи ДНК. Может быть, это объясняется тем, что фермент AID каким-то образом отличает верхнюю цепь от нижней и дезаминирует цитозины только в верхней цепи? Авторам удалось показать, что это не так, что цитозины обеих цепей подвергаются дезаминированию в равной степени. Однако в нижней цепи это приводит к замене другим нуклеотидом только самого цитозина, а в верхней – также и к замене многих соседних нуклеотидов.
Особенно часто мутации происходят на расстоянии в 4–15 нуклеотидов по обе стороны от дезаминированного цитозина в верхней цепи. По мнению авторов, ключевую роль здесь играет система репарации (починки) ДНК. Белки, осуществляющие репарацию, находят в верхней цепи дезаминированный цитозин (урацил) и начинают «исправлять ошибку». Вероятно, они при этом вырезают довольно большой кусок ДНК вокруг «испорченного» нуклеотида, а потом не слишком аккуратно его восстанавливают. Так и появляются многочисленные мутации. По-видимому, за починку верхней и нижней цепи отвечают разные системы репарации, причем первые работают с ошибками, а вторые – без. При помощи ряда дополнительных экспериментов ученым удалось выявить конкретные белки, ответственные за «неаккуратную починку» верхней цепи ДНК в V-областях (Msh2/6, Exo1, ДНК-полимераза η).
Данное исследование – важный шаг к пониманию того, каким образом живая клетка может контролировать изменения собственного генома. Однако вопросов по-прежнему остается много. Например, очень хотелось бы узнать, каким образом фермент AID находит V-область и как клетка определяет, к каким из «испорченных» нуклеотидов нужно направить точные, а к каким – склонные к ошибкам системы репарации. Наконец, эволюционистов-теоретиков не может не волновать крамольный вопрос: что если механизм гипермутирования иногда включается не только в лимфоцитах?
Источник: Shyam Unniraman, David G. Schatz. Strand-Biased Spreading of Mutations During Somatic Hypermutation // Science. 2007. V. 317. P. 1227–1230.
Александр Марков, http://elementy.ru





